
realreal
-
Innlegg
76 -
Ble med
-
Besøkte siden sist
Innholdstype
Profiler
Forum
Hendelser
Blogger
Om forumet
Innlegg skrevet av realreal
-
-
Ops, mente "ikke pentan-3-on". Vet det var pentan-3-on som ga to topper i H-NMR spekteret. Mente den andre fraksjonen
Jeg svarte pentan-2-ol. Eneste med kokepunkt innenfor området

-
Hva skrev dere på hvorfor svovel syre brukes i reaksjonen
Jeg argumenterte for at
Svovelsyre er vanntiltrekkende, og i følge Le cheatuleres prinsipp så vil dette forskyve likevekten mot høyre (ettersom at vann blir "borte") Og dermed vil vi få mer at produktet. noe sånt
Noen andre?
Akkurat samme



Fikk dere også heksan-3-on på del 1? Eller var det pentan-3-on
Pentan-3-on ja, den som hadde bare to ulike hydrogenmiljø
-
Hva skrev dere på hvorfor svovel syre brukes i reaksjonen
Jeg argumenterte for at
Svovelsyre er vanntiltrekkende, og i følge Le cheatuleres prinsipp så vil dette forskyve likevekten mot høyre (ettersom at vann blir "borte") Og dermed vil vi få mer at produktet. noe sånt
Noen andre?
Akkurat samme

-
0,0625 tror jeg
glemte du å gange med 2? Vi hadde 0,5L, bufferkapasitet er 1L
0,11 LHva fikk dere på den aller siste oppgaven? Den med hvor mange 1,0 mol/L saltsyre som kunne tilsettes?
Skulle ikke finne bufferkapasitet, men antall liter på denne bufferen
 Som var på 0,5 L
Som var på 0,5 LMen i oppgaven før, hva fikk dere at skulle bli stoffmengden til den sure komponenten?

Samme her
 Eller, 0,0626 da
Eller, 0,0626 daMen dette er etter at likevekten innstilte seg, sant?

Jepp
 Tilsatte 15,76g NaHCO3 = 0,1876 mol
Tilsatte 15,76g NaHCO3 = 0,1876 mol -
Noen som har eksamen?
Forresten hvor mange g metanol trengte dere for å få 1 kg brommetan
jeg fikk 354 g ish
355g

Bra,
Oppgave 3.
Den hvor mye jern som var, den første var rundt 1,2 kg hvis jeg ikke tar feil, og den rett under var 0.5 g, at elevene hadde like mye.
Hva fikk du?
Jeg fikk 0,4999g --> 0,50g, altså at det var rent jern ja
 På den første fikk jeg 1,3 kg :/
På den første fikk jeg 1,3 kg :/ -
Noen som har eksamen?
Forresten hvor mange g metanol trengte dere for å få 1 kg brommetan
jeg fikk 354 g ish
355g

-
Forslag til løsninger oppgave 1:
Hvis det stemmer har jeg alle riktig!

-
 1
1
-
-
Det sto regn ut hvor mange mye 1 mol/l Saltsyre vi trenger
Åja, daså. Skrev at vi trengte 0.22 per liter. Jeg vet ikke hvorfor jeg tenkte bufferkapasitet

Ei i klassen min som gjorde det samme... Det står jo ordet bufferkapasitet, kanskje lett å tenke sånn :/
-
Hva fikk dere på den aller siste oppgaven? Den med hvor mange 1,0 mol/L saltsyre som kunne tilsettes?
0,11 L
glemte du å gange med 2? Vi hadde 0,5L, bufferkapasitet er 1L
Skulle ikke finne bufferkapasitet, men antall liter på denne bufferen
 Som var på 0,5 L
Som var på 0,5 LMen i oppgaven før, hva fikk dere at skulle bli stoffmengden til den sure komponenten?
0,0625 tror jeg

Samme her
 Eller, 0,0626 da
Eller, 0,0626 da -
Hva fikk dere på den aller siste oppgaven? Den med hvor mange 1,0 mol/L saltsyre som kunne tilsettes?
0,11 L
glemte du å gange med 2? Vi hadde 0,5L, bufferkapasitet er 1L
Skulle ikke finne bufferkapasitet, men antall liter på denne bufferen
 Som var på 0,5 L
Som var på 0,5 L -
Hva fikk dere på den aller siste oppgaven? Den med hvor mange 1,0 mol/L saltsyre som kunne tilsettes?
0,11 L
-
Hva svarte du på avkrysningene?
Jeg svarte: CACCDACBDAACDDBBCACB
-
 1
1
-
-
Men vil ikke absorbansen også påvirkes av alle de andre forbindelsene jord består av? Med konsentrasjonen av etanol i en vannledning kan det tilsettes en fargeindikator, og ettersom det er i vann, så vil ikke absorbansen påvirkes i like stor grad av andre forbindelser i vannet. eller er jeg helt på jordet?
Ville svart A, siden nitkkelioner har farge. Har ikke hørt om kolorimetri i sammenheng med pH eller organiske forbindelserHva ville dere ha svart på denne?
Kolorimetrisk analyse er en godt egnet metode for å finne:
A: nitratinnholdet i en jordprøve
B: pH-verdien i en saltsyreløsning
C: konsentrasjonen av etanol i en vannløsning
D: bufferkapasiteten til en jordprøve
Jeg mener altså at C ville VærT riktig.
Mener det er underforstått at man først må isolere ionene fra jordløsningen på en eller annen måte? Men kanskje du har rett

-
Hva ville dere ha svart på denne?
Kolorimetrisk analyse er en godt egnet metode for å finne:
A: nitratinnholdet i en jordprøve
B: pH-verdien i en saltsyreløsning
C: konsentrasjonen av etanol i en vannløsning
D: bufferkapasiteten til en jordprøve
Ville svart A, siden nitkkelioner har farge. Har ikke hørt om kolorimetri i sammenheng med pH eller organiske forbindelser
-
En kjapp spm. Når proteiner denaturerer, er det primær- sekundær-, tertiær-, eller kvartiærstrukturen som ødelegges?
Det mister sin tredimensjonal struktur, altså sekundær, tertiær og kvartær-struktur
-
Vår 2013 oppgave r) del 1 noen?
Hvorfor er B riktig svar? Er ikke alle salter med NO3 lettløselige? Burde ikke B på bakgrunn av det være uaktuell? Stoffet Ni(NO3)2 altså.
Nei, det utelukker det ikke, det står ikke at alt må felles ut, bare at noe ikke løser seg i vann. Det du vet er at minst ett av saltene ikke har lav løselighet, og at det må være karbonat til stede. Dermed er bare B aktuell.
-
Kan jordalkali (eg: Ca) metaller benyttes i H2PO4(-) og HPO4(2-) og lignende syre-base par uten å påvirke pH i løsningen? I eksemplene jeg har sett så langt så har kun Na og Na2 blitt brukt.
Kalsiumsalter felles ut i mange tilfeller, feks med sulfat. Det er best å bruke natrium eller kaliumsalter, da de alltid er lettløselige
-
 1
1
-
-
Dere gjennomgikk ikke strips i kjemi 1? Tolkningen av strips er nokka av det verste..
Hva mener du med strips?
Jeg kan ikke huske at jeg hadde det som pensum i 2010. Da jeg hadde jeg eksamen i kjemi 2.
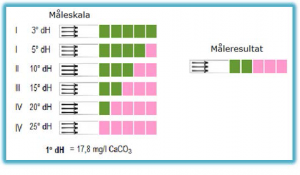
Det er ikke "pensum", men relativt enkelt å forstå likevel. I dette eksempelet er hardhetsgrad = 15 dH, så er det bare å regne om til kalsiumkonsentrasjon.
Konvertering mellom hardhetsgrad (dh) og kalsiumkonsentrasjon har iallefall jeg ikke lært. Og jeg fikk 6 i naturfag og kjemi 1.
Det står i boka vår (aschenhoug), og i tillegg så er det oppgitt konvertering i eksamensoppgaven. Bare se på bildet jeg la ut.
-
Dere gjennomgikk ikke strips i kjemi 1? Tolkningen av strips er nokka av det verste..
Hva mener du med strips?
Jeg kan ikke huske at jeg hadde det som pensum i 2010. Da jeg hadde jeg eksamen i kjemi 2.
Det er ikke "pensum", men relativt enkelt å forstå likevel. I dette eksempelet er hardhetsgrad = 15 dH, så er det bare å regne om til kalsiumkonsentrasjon.
-
-
Man er avhengig av å tenke litt selv, ikke bare lese av boka, for å få toppkarakter. F.eks på måling av hardt vann med strips kan de fleste tenke seg til at det blir høy feilmargin på svaret på grunn av en grov skala. Det står om Beer-Lamberts lov i boka vår, så det er litt rart siden det er så viktig. Det om kobbermalm må man jo også tenke litt selv rundt, på bildet ved oppgaven så man jo f.eks et enormt område som var "ødelagt" av utvinningen, og det var liten grad kobber i jordsmonnet uansett. Utslipp av avfall, kjemikalier, CO2 osv er nesten standard. Vi har også et kapittel om livsløpet til materialer i boka vår, hvor det f.eks står litt om gruvedrift.
Jada, jeg tenkte ikke å lese av boka heller, men når boka ikke nevner noe og vi ikke har gått gjennom det, er det helt håpløst.
Hvordan kunne jeg tenkt meg fram til det med strips? Jeg hadde jo aldri hørt om metoden engang før jeg så den eksamenen. Jeg kunne selvsagt nevnt det med at dert er en grov skala, men når jeg så i løsningsforslaget, var det mye mer detaljert. Det sto noe om at dH på 15 omfavner alt fra 12.4-17.5 dH elns. Da har jeg plutselig mista ett poeng.
Joda, skjønner det, særlig det med Beer-Lambert som var veldig rart. Tror ikke det er nødvendig å oppgi feilmarginen på stripsen, jeg tror nok det hadde holdt å si at det var en grov skala, hvor hvert trinn dekket et relativt stort område og at dette ga stor feilmargin.
-
Ok, nå er jeg rett og slett pisslei disse eksamenene. Det er FLERE oppgaver der de tar utgangspunkt i forsøk som ikke engang er nevnt i studieboka. F. eks 2014 siste oppgave del 2, skal vi nevne ulemper ved å bestemme konsentrasjon ved å bruke Strips. Har ikke vært borti det i timene, og boka nevner ikke det hele tatt. Jeg har Kjemi 2 boka fra Cappelendamm.
Så var det en oppgave om Beer-Lamberts Lov. OK. Boka nevner kolometri, ikke noe om Beer. Hadde et bittelite forsøk om det, og heller ingenting om Beer der heller.
Så kommer også oppgaver der du rett og slett skal synse. Så en oppgave om miljøutfordringer ved å utvinne malm. Fasiten? Jo, en A4-side om malm. Igjen, her også ingen oppslagsverk.
Jeg klarer kjemi i utgangspunktet ganske greit, og jeg tror jeg får 5 eller 6, men når jeg ser sånne drittoppgaver som det blir jeg bare oppgitt. Hva i huleste er det udir tenker???
Man er avhengig av å tenke litt selv, ikke bare lese av boka, for å få toppkarakter. F.eks på måling av hardt vann med strips kan de fleste tenke seg til at det blir høy feilmargin på svaret på grunn av en grov skala. Det står om Beer-Lamberts lov i boka vår, så det er litt rart siden det er så viktig. Det om kobbermalm må man jo også tenke litt selv rundt, på bildet ved oppgaven så man jo f.eks et enormt område som var "ødelagt" av utvinningen, og det var liten grad kobber i jordsmonnet uansett. Utslipp av avfall, kjemikalier, CO2 osv er nesten standard. Vi har også et kapittel om livsløpet til materialer i boka vår, hvor det f.eks står litt om gruvedrift.
-
Hvordan ville dere ha vurdert utsagnet: «Bufferkapasiteten er størst ved halvtitreringspunktet.»?
Kort og greit ville jeg svart at vi har en ideell buffer når [base]=[syre], for det skal like store mengder sterk syre og base til for å ødelegge bufferen. Det betyr ikke nødvendigvis at bufferkapasiteten er størst ved halvtitreringspunktet, for bufferkapasiteten avhenger av om vi velger å regne bufferkapasiteten med hensyn på enten syre eller base.
I følge løsningsforslaget er bufferkapasiteten størst ved halvtitreringspunktet, men jeg er litt uenig der. Noen innspill?
Skjønner hva du tenker på, for dersom pH > pKa vil jo bufferkapasiteten med hensyn på syre være større enn ved pH = pKa. Men, vii har lært av vi må regne bufferkapasiteten til den "siden" hvor kapasiteten er minst, med mindre noe annet er oppgitt i oppgaven. Dermed vil bufferkapasiteten være størst når pH = pKa (halvtitrerpunktet).
-
Hei, noen som har gjort høst 2013-eksamen? På oppgave 5c) står det i "fasiten" at den molare massen til bly(II)acetat er 301,26 g/mol, og at hydratisert bly(II)acetat (3H2O) har molar masse 355,32 g/mol. Det stemmer ikke med mine utregninger, andre som får feil der?
Pb(ChCOO)2 * 3H2O mM=
207,2+4*12,01+4*16+2*1,008+3*1,008+3*16= 372,28 g/molDet er det samme som jeg fikk! Må være feil i fasit?

Kjemi eksamen våren 26 mai 2015
i Skole og leksehjelp
Skrevet
Men løsningsforslaget sa at A var riktig?